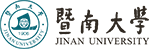近日,暨南大学雷文亮研究员与陈功教授团队在国际权威期刊《Advanced Science》(IF=14.1)发表一项重要研究成果。该研究题为“A NeuroD1 AAV-Based Gene Therapy for Functional Brain Repair in Alzheimer’s Disease-Like Non-Human Primate Model”,首次在阿尔茨海默症样成年猕猴模型中系统研究了NeuroD1基因疗法的多重修复作用,发现该疗法可诱导星形胶质细胞原位高效转化为神经元,同时显著抑制神经炎症反应、修复血脑屏障、延缓海马萎缩,并恢复认知功能,从而在脑组织、脑影像、和行为学等多维度实现了阿尔茨海默症的有效逆转,为全球数千万的阿尔茨海默症患者带来了新希望。

阿尔茨海默症(Alzheimer’s disease, AD)会逐渐侵蚀患者的记忆与认知功能,已成为全球数千万家庭难以承受的重负。过去数十年间,尽管科学界和工业界投入巨大,但目前获批的AD疗法仍以缓解症状为主,无法从根本上阻止神经元的持续丢失与脑组织的进行性萎缩。陈功教授团队长期从事基于神经转录因子将脑内星形胶质细胞原位转化为功能性神经元的开创性研究,并在一系列啮齿类神经疾病模型上取得了丰硕的成果。为精准模拟人类阿尔茨海默症的病理进程,研究团队在猕猴海马脑区特异性过表达人源tau蛋白(hTau),导致神经元进行性丢失、炎症反应增强、血脑屏障损伤、以及记忆功能下降等一系列AD样表型,为后续治疗性研究提供了一个能模拟中到重度AD患者的病理模型。
基于这一灵长类大动物AD样模型,研究团队将编码NeuroD1的AAV载体直接注入因tau蛋白过表达而导致大量神经元死亡的海马脑区,发现星形胶质细胞能够原位高效转化为神经元,且观察到明确的中间态细胞,为直接转分化提供了关键证据。更为重要的是,这一细胞层面的转变最终转化为结构与功能的多维度修复:NeuroD1治疗后,神经元密度显著增加,海马萎缩被成功遏制;神经炎症得到有效缓解,胶质细胞活化水平明显下降;血脑屏障功能得到修复,脑脊液中的AD相关生物标志物也显著改善。在功能层面,海马区的葡萄糖代谢水平明显提升,对应着神经功能的恢复;同时,动物的空间工作记忆持续改善。该研究为NeuroD1基因疗法迈向临床应用提供了关键的临床前灵长类大动物证据。
随着人口老龄化进程加速,阿尔茨海默症的发病率持续攀升。然而,过去二十年间,几乎没有新机制药物能够真正逆转AD疾病进程。NeuroD1基因疗法在非人灵长类AD模型中的成功,不仅为阿尔茨海默症患者提供了新的治疗方法,也为一系列因为神经元死亡而导致的重大神经疾病的治疗开辟了一条全新的原位神经再生途径。该灵长类研究标志着人类或将从单纯延缓神经退行性疾病迈向脑组织与功能修复逆转的新阶段。目前,基于该项灵长类大动物的研究,陈功教授创办的神曦生物公司(NeuExcell Therapeutics)已经与安徽省立医院(中科大第一附属医院)施炯教授团队合作开展了临床研究(IIT),并在部分患者身上观察到了令人欣喜的初步疗效。
本研究由暨南大学粤港澳中枢神经再生研究院雷文亮研究员和陈功教授为共同通讯作者,博士研究生降周权和覃永鹏为本文共同第一作者,技术员罗斌和白帆也为本研究做出重要贡献。该项工作受到广东省珠江人才团队、广州市脑科学重点研究计划、广州市科技局、暨南大学、暨南大学附属第一医院,暨南大学生物活性分子与成药性优化全国重点实验室等支持。